Memahami struktur atom merupakan langkah awal yang sangat penting dalam mempelajari ilmu Fisika secara lebih mendalam. Sebagai salah satu konsep dasar, teori atom tidak hanya menjelaskan apa yang menyusun segala materi di sekitar kita, tetapi juga menjadi fondasi bagi berbagai penemuan ilmiah lainnya.
Untuk memperluas wawasan serta mengenal lebih jauh bagaimana atom tersusun dan bagaimana perkembangannya dari masa ke masa, berikut penjelasan lengkap mengenai teori struktur atom, model-model atom, hingga kaitannya dengan tabel periodik.
Pengertian Struktur Atom
Atom adalah bahasa yang berasal dari bahasa Yunani, yaitu “Atomos”. Kata Atom sendiri memiliki arti “tidak dapat dibagi”. Democritus adalah orang Yunani pertama yang mengemukakan konsep dasar dari atom di awal abad ke-4 sebelum masehi. Dalam hal in, Democritus mengungkapkan bahwa atom adalah benda dapat dibagi menjadi beberapa bagian yang sangat kecil sampai akhirnya tidak dapat dibagi.
Teori atom ini juga mengatakan bahwa atom tidak memiliki bentuk yang sepenuhnya padat, namun atom sendiri memiliki struktur internal yang memiliki ruang kosong antara atom untuk pergerakan yang akan di lakukannya. Hal ini yang membuat atom dapat bergerak dalam air dan udara, bahkan memiliki gerakan yang fleksibilitas dalam bentuk beda padat.
Atom sendiri juga dapat dibedakan dalam bentuk, masa dan juga ukurannya. Dalam hal ini, atom juga memiliki perbedan dari sifat dan bagaimana materialnya. Untuk model yang dibuat oleh Democritus sendiri, dijelaskan bahwa atom adalah benda yang semua bentuknya memiliki ukuran yang kecil. Namun teori ini belum memiliki bukti eksperimental yang kuat sehingga masih muncul teori baru.
Pada tahun 1800an yang membuat teori-teori mengenai atom akhirnya muncul dengan didasarkan eksperimen yang dilakukan. Hal ini juga yang membuat atom dikenal sebagai satuan kecil sebuah materi yang mana dapat berupa benda beragam, seperti cair, padat dan juga gas. Atom sendiri merupakan bentuk dari bahan dasar yang membentuk sebuah materi sampai ke bentuk yang dapat di rasakan.
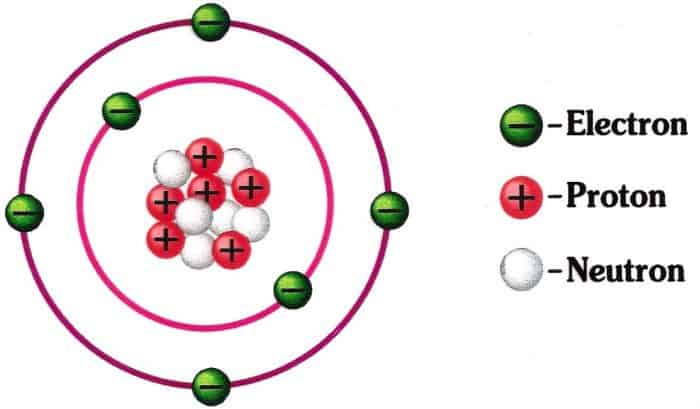
Materi tersebut seperti gas dan juga angin, untuk benda atom dapat berupa seperti air, kayu dan juga handphone. Struktur atom sendiri terdiri atas 3 inti materi, yaitu elektron, proton dan juga neutron. Ketiga ini adalah inti yang berada dalam inti atom. Namun elektron adalah bagian inti yang mengelilingi atom seperti proton dan juga neutron.
Ketiga struktur atom ini memiliki muatan yang berbeda. Proton memiliki struktur atom yang bermuatan positif, neutron untuk muatan netral dan juga elektron yang bermuatan negatif. Hal ini juga yang membuat struktur atom berada dalam sistem periodik yang dipengaruhi oleh daya tarik elektron, proton dan neutron.
Struktur Atom John Dalton

Pada tahun 1803, John Dalton pertama kali mengemukakan pendapatnya mengenai struktur atom. Dalam hal ini, tentunya teori yang dikemukakakn oleh Dalton didasarkan pada dua hukum, yaitu hukum susunan tetap atau yang lebih dikenal dengan hukum prouts dan hukum kekekalan masa atau hukum Lavoisier.
Kedua hukum ini memiliki pernyataan yang berbeda, dimana untuk Lavosier menyatakan, “reaksi akan selalu sama dengan masa total zat-zat engan masa total zat hasil dari reaksi”. Sedangkan untuk prouts menyatakan bahwa, “setiap perbandingan yang dimiliki oleh unsur dalam suatu senyawa akan selalu tetap”. Dari kedua teori ini, maka Dalton menyimpulkan struktur atom bahwa :
- Atom adalah salah satu bagian yang paling kecil yang dimiliki materi dan tidak dapat untuk dibagi
- Atom dapat digambarkan sebagai salah satu bola pejal yang berukuran kecil
- Atom bergabung dengan senyawa lainnya dengan perbandingan untuk bilangan bulat dan memiliki bentuk sederhana
Kelebihan struktur atom Dalton:
Membangkitkan keinginan untuk para peneliti untuk melakukan penelitian lebih jauh mengenai model atom
Kelemahan struktur atom Dalton:
Teori ini adalah salah satu teori yang mana tidak dapat memberikan kejelasan mengenai larutan yang dapat menghantarkan listrik.
Struktur Atom JJ.Thomson

Teori ini dikemukakan oleh salah satu peneliti bernama JJ.Thomson. Thomson mengatakan pendapatnya bahwa atom sendiri memiliki dua partikel yang bernama elektron dan juga proton. Dalam hal ini Thomson juga melakukan eksperimen yang menghasilkan bahwa proton memiliki masa yang lebih besar dibandingkan dengan elektron, inilah yang membuat Thomsosn menggambarkan atom sebagai proton.
Namun di dalam proton sendiri, adanya elektron memiliki fungsi untuk memberikan nilai neral terhadap positif dari proton. Kesimpulan didapatkan bahwa Thomson, berpendapat bahwa atom adalah bola pejal positif namun memiliki muatan negatif yang tersebar di dalamnya. Struktur atom yang di kemukakakn oleh Thomson ini memiliki kelebihan dan kekurangan.
Kelebihan struktur atom J.J Thomson:
Dapat memberikan bukti bahwa adanya partikel lainnya yang juga memiliki nilai negatif. Hal ini juga muncul kesimpulan bahwa atom bukan merupakan satu-satunya bagian yang paling kecil dari suatu unsur.
Kelemahan struktur atom J.J Thomson:
Model ini tidak dapat menjelaskan secara rinci mana yang merupakan susunan positif dan negatif dari bola tersebut. Hal ini tentunya akan memudahkan perhitungan yang akan di lakukan untuk penghitungan model atom.
Struktur Atom Rutherford
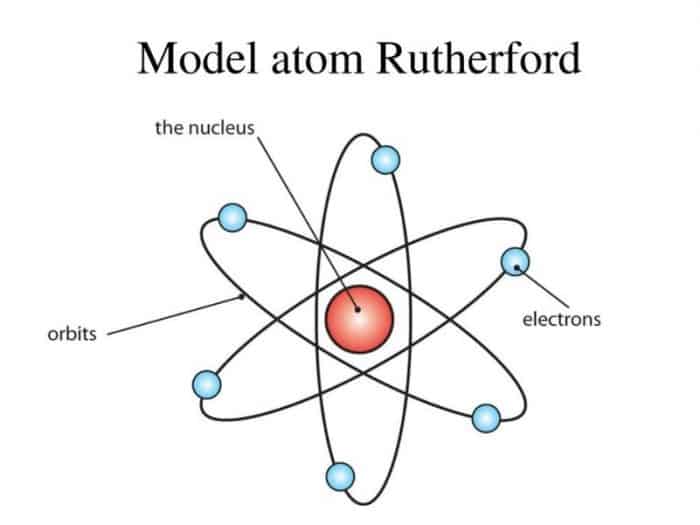
Struktur atom ini mulai dikemukakan oleh Rutherford. Namun dia tidak sendiri, melainkan bersama dengan kedua muridnya dan melakukan percobaan dengan hamburan sinar alfa terhadap lempeng tipis emas. Dalam percobaan yang dilakukannya, dihaslilkan kesimpulan bahwa partikel alfa dapat menembus lembaran emas tanpa adanya belokkan.
Bukan hanya itu, Rutherford juga menemukan partikel alfa lainnya yang dibelokkan sedikit dan memberikan hasil yang cukup mengejutkan, yaitu partikel alfa tersebut kembali langsung menuju sumber radioaktif. Dalam hal ini, untuk memberikan dan melihat lebih jauh lagi Rutherford melakukan uji coba dengan mengemabngkan model inti atom.
Dengan percobaan yang dilakukannya, kesimpulan yang di dapat yaitu Atom bukanlah merupakan bola pejal., dikarenakan hampir semua partikel alfa diteruskan. Kesimpulan lainnya yaitu lempengan emas yang ada dianggap sebagai satu lapisan atom emas yang mana memiliki partikel atom yang sangat kecil dengan muatan posiif.
Kesimpulan terakhir yaitu bahwa partikel tersebutlah yang menyusun inti dari atom. Hal ini tentunya di dasarkan dengan fakta dimana 20.000 partikel alfa yang ada akan dibelokkan. Dari kesimpulan yang didapat, Rutherford yakin bahwa atom sendiri terdiri dari inti atom yang mana memiliki ukuran sangat kecil dan muatan yang ada positif, namun dikelilingi oleh muatan negatif.
Kelebihan struktur atom Rutherford:
Atom adalah salah susunan dari inti atom dan juga elektron yang mana mengelilimgi inti. Mengelilingi inti ini juga merupakan gerakan yang mana memberikan inspirasi pada penemuan baru lainnya yaitu tentang lintasan atau kedudukan elektron yang lebih dikenal sebagai kulit elektron.
Kekurangan struktur atom Rutherford:
Belum ada penjelasan yang pasti mengenai bagaimana elektron dapat jatuh ke dalam inti atom. Dalam hal ini, jika di dasarkan dengan teori gerak, maka elektron mengitari inti bersamaan dengan pemancarana energi yang akan lama. Hal ini akan membuat energi dari elektron berkurang dan makin lama akan mendekati inti dan jatuh kedalamnya.
Model Atom Niels Bohr
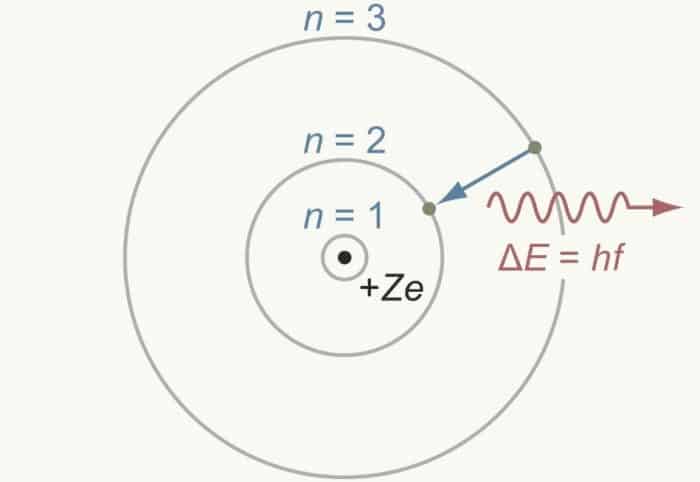
Strujtur atom ini muncul di tahun 1913, dimana saat itu Niels Bohr mencoba untuk memperbaiki beberapa kegagalannya dalam uji coba spectrum atom hydrogen. Dalam hal ini, hasil percobaannya menunjukan bahwa kedudukan orbit elektron menempati daerah yang ada di sekitar inti. Menurut Niels Bohr, inti atom di kelilingi oleh elektron yang mana berada pada orbit tertentu.
Namun hanya beberapa orbit yang memiliki jumlah tertentu, antara orbit satu dengan orbit lainnya memiliki jarak orbit sendiri dari inti atom. Tingkatan energi yang dimiliki elektron juga mempengaruhi keberadaan elektron, baik untuk orbit yang berada dalam titik rendah maupun titik yang tinggi. Hal ini juga yang membuat sebuah elektron yang ada di orbit rendah dan energi yang dimilikinya kecil.
Hal ini membuat Niels Bohr mengemukakan pendapatnya secara garis besar terhadap penelitian yang di lakukannya, yaitu:
- Elektron sendiri adalag sebuah atom yang mana memang bergerak untuk mengelilingi intinya pada lintasan-lintasan tertentu. Dalam hal ini, elektron sendiri tidak memancarkan energi dan disebut sebagai kulit atau tingkat energi elektron.
- Bukan hanya menetap, melainkan elektron sendiri dapat berpindah dari tingkat energi yang memiliki tingkatan yang tinggi dank e rendah disertai dengan pemancaran energi yang ada. Namun untuk perpindahan energi dari energi yang memiliki tingkat yang rendah ke tinggi, hal ini disertai dengan penyerapan tinggi.
- Elektron yang bergerak dalam hal ini pada lintasannya berada pada keadaan elektron yang tidak memancarkan energi apapun. Bukan hanya tidak memancarkan, melainkan tidak menyerap energi.
Hal ini yang membuat Niels Bohr mengungkapkan dan berpendapat bahwa elektron-elektron atom yang mana mengelilingi inti pada lintasan tersebut disebut dengan kulit elektron atau tingkat energi. Untuk tingkat energi yang paling rendah, merupakan kulit elektron yang mana terletak di bagian paling dalam. Sednagnya untuk bagian paling luar dan semakin keluar, memiliki energi yang semakin besar juga.
Kelebihan struktur atom Niels Bohr:
Atom Niels Bohr memiliki pengertian yaitu atom yang mana terdiri dari beberapa kulit untuk melakukan perpindahan elektron yang ada.
Kelemahan struktur atom Niels Bohr:
Salah satu kelemahan model atom ini adalah tidak dapat menjelaskan apa itu efek Zeeman dan efek Strack. Hal ini juga yang membuat efek ini tidak dapat dibuktikan secara lebih jelas.
Struktur Atom Fisika Modern
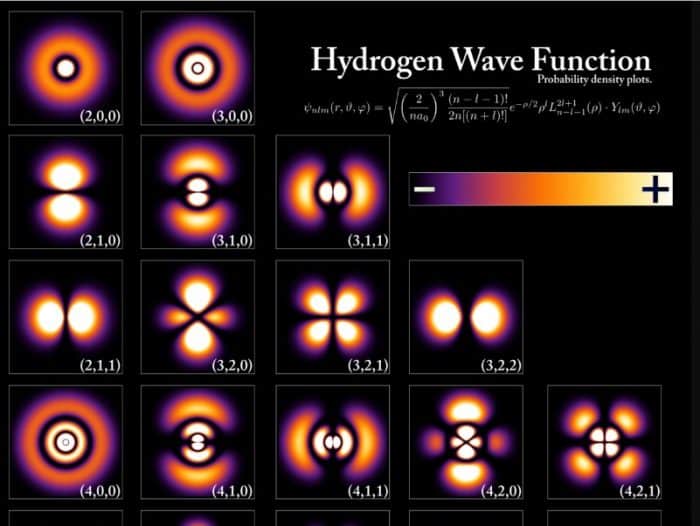
Pengertian dasar dari atom sendiri adalah atom yang memang terdiri dari elektron, proton dan juga neutron. Dalam hal ini, ada kemungkinan bahwa struktur atom yang akan dibuat lebih sulit dan rumit karena lengkap mengenai bagaimana keadaan atom yang saat ini masih dianggap belum adanya kejelasan.
Erwin Schrodinger merupakan salah seorang yang mana menjelaskan mengenao struktur atom fisika modern. Dalam hal ini sebelum Erwin, seorang ahli Jerman bernama Werner Heisenberg juga mengembangkan teori mekanika kuantum yang lebih dikenal sebagai prinsip ketidakpastian.
Prinsip ini mengemukakan bahwa tidak mungkin untuk menentukan kedudukan dan momentum sebuah benda secara bersamaan, namun yang dapat di tentukan adalah kebolehjadian suatu elektron yang mana memiliki jarak tertentu dari inti sebuah atom. Salah satu ciri khas yang dimiliki oleh model struktur atom ini adalah memiliki orbital lintasan elektron.
Struktur Atom Isotop
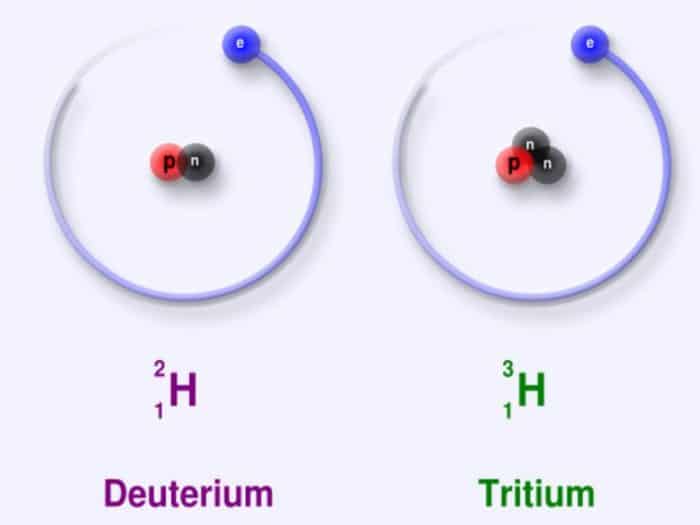
semua atom yang mana berasal dari masa atom memiliki nomor atom yang identik. Dalam hal ini, masa yang dimiliki juga berbeda-beda. Isotop sendiri memiliki atom-atom yang mana sama dengan nomor atom lainnya namun memiliki perbedaan dengan nomor masa. Dalam hal ini, dapat dikatakan jika semua unsur memang memiliki alam yang berbeda, namun pada umumnya memiliki campuran isotope-isotop.
Hal ini juga yang menghasilkan berbagai perhitungan yang perlu diketahui rata-rata yang dimilikinya beraal dari masa-masa isotope-isotop unsur yang ada di alam. Unsur-unsur ini tentunya di dasarkan atas kelimpahan yang dimiliki oleh masing-masing isotope tersebut yang ada di alam dalam masa yang disebut masa atom.
Struktur Atom Isobar dan Isoton
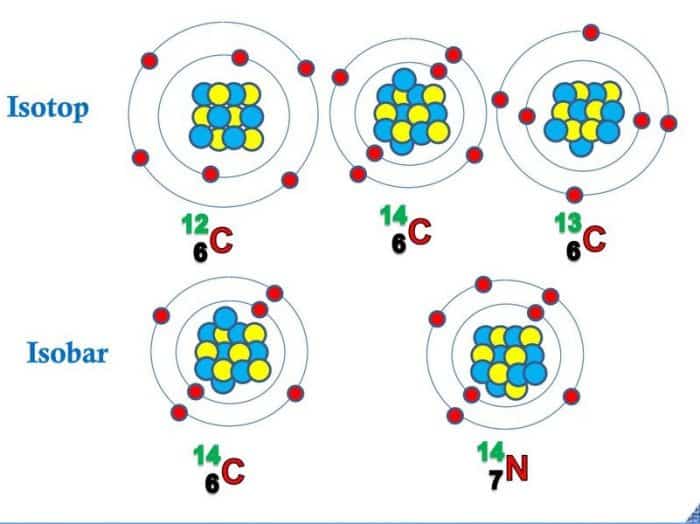
Struktur atom yang dimiliki isobar dan juga isoton memiliki masa yang sama, namun memiliki nomor yang berbeda. Nomor tersebutlah yang membedakan antara isobar dan juga isoton. Isobar dapat diartikan sebagai atom-atom yang mana memiliki nomor masa yang nama dengan isoton, namun memiliki nomor atom yang berbeda. Dalam hal ini berbeda dengan isoton.
Isoton adalah atom-atom yang mana memiliki jumlah neutron yang sama dengan isobar, namun memiliki nomor atom atau unsur yang berbeda.
Struktur Atom dan Tabel Periodik
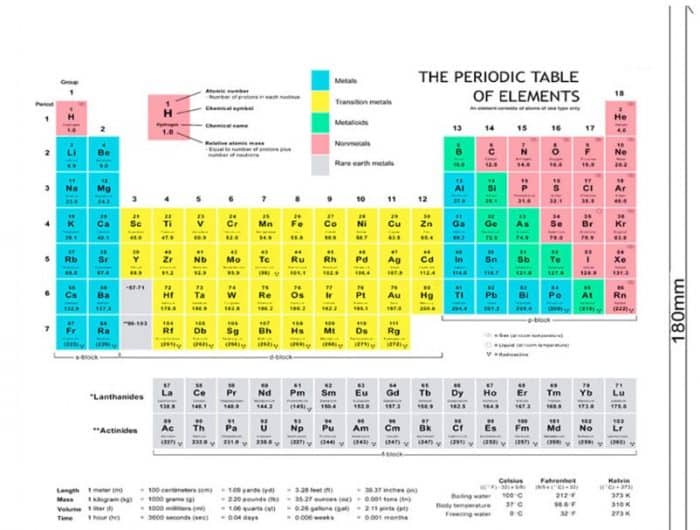
1. Partikel dasar yang menyusun atom
Atom sendiri sudah dikenal sebagai bagian yang paling kecil dalam suatu unsur. Dalam hal ini, struktur atom juga memiliki fungsi untuk menggambarkan bagaimana partikel yang dimiliki oleh atom dapat di susun. Nantinya atom akan tersusun dari inti atom bahkan hingga elektron yang memang mengelilingi atom tersebut. Elektron itu nantinya akan tersebar di kulit atom.
Sebagian besar untuk atom sendiri juga terdiri dari berbagai ruang hampa. Di dalam ruangan hampa tersebut memiliki inti yang ukurannya sangat kecil, dimana masa dan juga muatan positif yang dimilikinya akan dipusatkan dan juga di kelililingi oleh elektron yang memiliki muatan negatif. Inti atom sendiri terdiri dari proton dan juga elektron yang memiliki muatan yang berbeda.
Ketiga partikel yang dimiliki oleh atom, yaitu proton, neutron, dan elektron dikenal dengan lambang :
– X : untuk lambang suatu unsur
– Z : Nomor atom
– A : nomor masa
Itulah gambaran yang ada dalam table periodic.
2. Susunan dari sebuah atom
- Cobalah untuk melihat nomor yang terdapat pada table periodic. Dalam hal ini, anda dapat melihat tanda yang sebelumnya sudah dijelaskan. Nomor atom memiliki nomor yang selalu lebih kecil dibandingkan dengan nomor masa.
- Dalam hal ini, nomor atom adalah bentuk dari jumlah proton. Hal ini dikarenakan sifat atom yang netral, maka nomor atom juga merupakan jumlah dari elektron yang ada.
- Cobalah perhatikan susunan-susunan elektron yang ada dalam level-level enetrgi yang ada. dalam hal ini, selalu isi level yang berada paling dalam akan mengisi bagian yang paling luar.
- Perhatikan selalu bahwa jumlah tingkatan elekron yang paling luar dalam table periodic akan sama dengan nomor golongan yang memang memiliki dua elektron.
Kesimpulan
Struktur atom merupakan salah satu materi dasar dalam Fisika yang sangat penting untuk dipahami karena menjadi landasan dalam mempelajari berbagai konsep lainnya. Sejarah perkembangan teori atom menunjukkan bahwa pemahaman manusia tentang atom mengalami proses panjang, mulai dari gagasan awal Democritus yang menyatakan bahwa atom adalah bagian terkecil yang tidak dapat dibagi, hingga teori modern yang menjelaskan atom sebagai sistem kompleks dengan elektron, proton, dan neutron.
Berbagai ilmuwan telah memberikan kontribusi besar dalam mengembangkan model atom, mulai dari Dalton dengan model bola pejal, Thomson dengan teori atom bermuatan positif yang di dalamnya terdapat elektron, Rutherford dengan model inti atom, Bohr yang memperkenalkan konsep lintasan atau kulit elektron, hingga teori mekanika kuantum oleh Schrodinger dan Heisenberg yang menjelaskan keberadaan elektron secara kebolehjadian dalam orbital.
Pemahaman tentang isotop, isobar, dan isoton semakin memperkaya pengetahuan mengenai keragaman atom di alam, sedangkan tabel periodik membantu menggambarkan susunan partikel dasar serta sifat-sifat unsur berdasarkan nomor atom dan nomor massanya. Pelajari wawasan nusantara untuk menambah pengetahuanmu!
Secara keseluruhan, mempelajari struktur atom membantu kita memahami bahwa setiap materi tersusun dari partikel-partikel kecil dengan karakteristik tertentu. Melalui teori-teori yang terus berkembang, ilmu pengetahuan mampu memberikan gambaran yang semakin jelas mengenai bagaimana atom bekerja dan membentuk berbagai jenis materi di sekitar kita.
